elisa实验步骤 ELISA实验步骤有哪些
大家好,关于elisa实验步骤很多朋友都还不太明白,不过没关系,因为今天小编就来为大家分享关于ELISA实验步骤有哪些的知识点,相信应该可以解决大家的一些困惑和问题,如果碰巧可以解决您的问题,还望关注下本站哦,希望对各位有所帮助!
本文目录
elisa的原理和实验步骤
1.ELISA的原理
ELISA的基础是抗原或抗体的固相化及抗原或抗体的酶标记。结合在固相载体表面的抗原或抗体仍保持其免疫学活性,酶标记的抗原或抗体既保留其免疫学活性,又保留酶的活性。在测定时,受检标本(测定其中的抗体或抗原)与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与液体中的其他物质分开。再加入酶标记的抗原或抗体,也通过反应而结合在固相载体上。此时固相上的酶量与标本中受检物质的量呈一定的比例。加入酶反应的底物后,底物被酶催化成为有色产物,产物的量与标本中受检物质的量直接相关,故可根据呈色的深浅进行定性或定量分析。由于酶的催化效率很高,间接地放大了免疫反应的结果,使测定方法达到很高的敏感度。
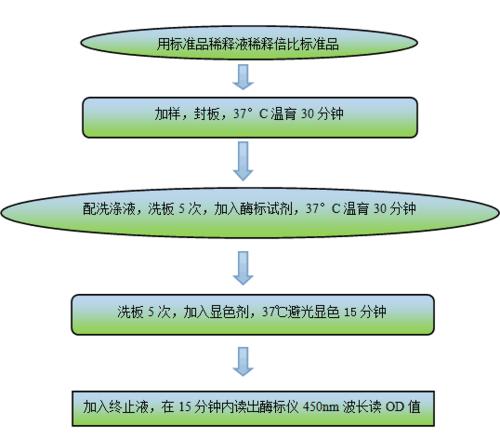
操作步骤:
1.从已平衡至室温的密封袋中取出试验所需板条,未用的板条和干燥剂请放回铝箔袋内压实自封条,密封口袋,放回4℃。
2.空白孔加标准品和标本稀释液,其余相应孔中加标本或不同浓度标准品(100ul/孔),用封板胶纸封住反应孔,36℃孵箱孵育90分钟。
3.提前20分钟准备生物素化抗体工作液。
4.洗板5次。
5.空白孔加生物素化抗体稀释液,其余孔加入生物素化抗体工作液(100ul/孔)。用新封板胶纸封住反应孔,36℃孵箱孵育60分钟。
6.提前20分钟准备酶结合物工作液。避光室温(22-25)℃放置。
7.洗板5次。
8.空白孔加酶结合物稀释液,其余孔加入酶结合物工作液(100ul/孔)。用新封板胶纸封住反应孔,36℃孵箱,避光孵育30分钟。
9.打开酶标仪电源,预热仪器,设置好检测程序。
10.洗板5次。
11.加入显色底物(TMB)100ul/孔,避光36℃孵箱,避光孵育15分钟。
12.加入终止液100ul/孔,混匀后即刻测量OD450值(3分钟内)。在仪器保存读数结果并打印一份纸质结果。
13.实验完毕后将未用完的试剂按规定的保存温度放回电冰箱保存至有效期结束。
建议保存酶标板框,以备下次或者今后试验使用。
如何进行elisa实验的质量控制
中医大的吧?复制个给你吧,看有没帮助....1.1基本概念
1.1.1质量控制(Quaility Control,Q.C)
质量控制是监视全过程,排除误差,防止变化,维持标准化现状的一个管理过程。这
一过程是通过一个反馈环路进行的。
1)确定控制的对象;
2)规定控制对象的标准(预期值);
3)制定或选择控制方法和手段;
3)测量实际数据;
4)比较或较对实际数据与预期值之间的差异,并说明产生这一差异的原因。超出预
定误差范围,报警系发出信号,反馈通道中断。
5)采取行动,解决差异。恢复原状(原标准状态)的手段发挥作用。
质量控制主要采用质控图进行。质控图是把某一检验的性能数据与所计算出来的预期
的"控制限"进行比较的图。这种性能数据是在按规程正常进行时,按时间顺序而抽选出来
的,其目的是检测检验过程中变异的"可追查"性原因。"可追逆"性的误差原因,是指除去
随机误差以外的其他原因。"控制限"是通过统计计算出来的,在后我们将详细介绍(见
1.3.室内质控程序)。
1.1.2误差
实验误差分为三种:系统误差、随机误差和过失误差。
系统误差是指一系列测定结果与真值或靶值存在有同一倾向的误差,有明显的规律
性,可在一定条件下重复出现,是可以通过质控预防和校正的。
随机误差又称偶然误差,是一种偶然的、未能预料到的误差,是难以避免和校正的误
差。检验工作中随机误差的分布符合正态分布规律。
过失误差是人为的责任误差。通过加强实验室管理和开展质量控制工作是可以避免
的。
1.1.3正态分布及标准差
ELISA试验中,检验同一样本达20次以上时,就会发现这组数据(指测定结果的吸光
值)分布在均值两侧,大部分集中在均值附近。如果以测定值为横坐标,以出现的频率为
纵坐标作图,就可绘出一个呈钟形的曲线图。如图5-1,钟顶处为均值,其他值以均值为
中心对称分布,这就是正态分布。
换言之,当ELSIA检测同一样本达一定次数后所得的一组数据,其中靠近均值(X)的
±1SD范围内的数据,占该组数据的68%,在X±2SD范围内分布的数据占总体的95%,
在X±3SD范围内分布的数据占总体的99%。当我们要求检验结果在X±2SD范围内为合格
时,将有95%的数据可能合格。
1.1.4真值
用确切的、最理想的决定性方法测得的值,称为真值。真值一般是测不到的。通过可
靠的决定性方法测出的值,称为靶值,通常用靶值来表示真值的大小。
1.1.5准确度(accuracy)
是指测定结果与真值(或靶值)接近的程度。准确度不能以数字表示,往往用不准确
度来衡量。测定结果与靶值的偏离程度称为偏差,它表示该项检验的不准确度。
绝对偏差=检验的均值-真值(或靶值)
相对偏差=绝对偏差真值÷(或靶值)×100%
1.1.6精密度(Precision)
是指对同一样本重复测定时,每次测定结果与平均值的接近程度,即重复测定值之间
的符合程度。
1.1.7标准品
1、国际标准品由WHO或相应组织标定的,用肯定的、公认的、准确的物理或化学方法
测定的定值材料。
2、国际生物学活性标准品根据生物学反应由WHO或相应组织标定的国际活性单位的材
料。
3、参考标准血清国家标准化组织根据国际标准化生产的法定材料。可用于鉴定仪器和
鉴定方法准确性。
1.1.8临床决定性水平(clinical decision leuel)
当某个被测物的浓度达到某一水平时,临床医师必须采用医疗措施。被测物的这浓度
称为临床决定性水平。
1.2质量控制血清
质控血清是已有靶值的血清,在每次的常规检验中加入一份或数份,通过所得结果来
了解本次检验的情况。质控血清检验的结果如能控制其误差在一定范围内,就说明该检验
没有发生不允许的误差。如果出现超过允许误差范围的异常结果,提示该检验不合格,应
寻找原因,纠正后,重检待测标本。因此质控血清在质控工作中起重要作用。
1.2.1质控血清的使用
卫生部临床检验中心制备的乙肝标志物质控血清,可以在-20℃保持半年定值不变。
冰冻状态融化使用时,应先混匀,未用完部分可在4℃保存5天。不宜反复冰融或自行分
装。开展某项检验的室内质控工作需要的质控血清,一般按3-6个月用量准备。自制的不
定值质控血清,在一批质控血清将用完之前,需准备下一批质控血清。质控血清要求性能
稳定,较长期内效价不变,其理化性质应与病人样本相近,这样才能有效地起到监测作
用。
1.2.2临界值质控血清
质控制血清分定值和未定值两种。如只用一份质控血清定值,一般定在正常值与异常
值交界点上,定性测定时处于弱阳性水平,称为临界值。乙肝标志物临界值的制定,应按
临床要求,为临床提供统一的判断弱阳性的标准。
临界值质控血清可以作为试剂盒中的阳性对照品和阴性对照品以外的第三个对照品,它可
以灵敏地反映出试剂盒的检出水平,确保弱阳性反应的标本不漏检。
1.2.3质控血清的制备
每个实验室可以根据自己的条件,选用临床中心提供的质控血清,或按以下方法自己制备
本室使用的质控血清(以乙肝质控血清为例)。
1)收集新鲜的无溶血、无黄疸、无细菌污染的阳性血清。
2) 56℃加热10小时来活。
3)离心或过滤除去沉淀。
4)用10%的小牛血清或正常人血清(PBS缓冲液)将收集的血清稀释至所需的浓度。如
能用正常的人血清稀释更好,因其成份更接近于检测标本。
5)抽滤除菌。按一次使用的量分装小安瓿,封口,20℃保存备用。不可反复冻融。
被检物要求检出的水平常被认为是质控血清应选择的水平。如果该试验还有其它要
求,则应加所要求浓度的质控物。
6)标定含量。20-30次测定结果删除>±2SD数据的均值作为靶值,并与已知定值血清对
比测定。
1.3室内质量控制程序
临床检验的检测结果,每次或每天之间不可能没有误差。决定允许的误差范围,以临
床上不造成误诊与漏诊为准,通过以下步骤来确定质控范围。
1)最佳条件下的测定误差。
2)已知值的血清在常规检验条件下的误差。
3)未知值的血清在常规检验条件下的误差。
4)临床应用的要求。对任何一个试验都应确定一个允许的误差范围,前题是满足临床要
求。如允许误差定得过小,在临床上不存在任何意义,但为了符合该规定却要花费很大人
力、物力和时间。相反,如果将允许误差定得过大,将使监测系统察觉不到临床上要求检
出的误差,失去质控的意义。
1.3.1最佳条件下已知值质控血清变异(optimal conditions variance,简称OCV)的测定
在本实验室最佳条件下(包括操作者、试剂、仪器等)检测质控血清20-30次,测得
结果计算,求出该组数据的均值和标准差(SD)表示该实验室的最佳工作质量。
现举例说明HBsAg ELISA法检测时OCV的测定。使用的质控制血清为临界血清,
HBsAg浓度为5ng/ml。在该实验室中选择素质最好、操作最熟练的技术员进行认真地专门
测定,选用最佳的试剂盒,检测之前,将恒箱、加样器等认真校正、调校正、调试,使用
新的加样吸头等,即在最佳、最理想的条件下进行检测。除质控血清外同时测定阴性对照
品和阳性对照品。并作双份测定,得出2个吸光值(A值),求出X。连续作20次,求出20
个X,即X1……X20。从这20个数据中,求出OCV的X和SD。
1.3.2常规条件下已知值质控血清变异(routine conditions variance-known value,简称
RCVK)的测定。
做常规检验的技术人员,在常规检验的条件下,将质控血清放在常规检测样本中,进
行20次检验,结果计算同OCV法。一般认为RCV的SD在OCV的SD两倍范围内可以接受。
若太大应该查找原因,使其向OCV的SD值靠近。在改进实验室条件后(例如较正加样
器,纠正洗板操作,调正温育温度等),重新进行RCVK的测定。如果RCVK的SD值更
小,说明OCV不是最佳条件下测定的,应重新再测OCV。常规条件下,RCVK肯定要比
OCV大。通过质控控制各项条件,使RCVK的数据尽可能接近OCV值。RCVK的数据反映
该实验室日常工作的质量,用于作质控图,对室内检验的结果进行控制,每日检验的结
果,报告能否发出。
1.3.3常规条件下,未知值质控血清变异(routine conditions variancl-unknown value简称
RCVU)的测定
有时为了避免主观性,再作RCVU测定。
测定步骤同RCVK,但检测的操作者不知质控血清的定值,或在操作者不知哪份是质
控血汪清的条件下进行常规检验,以排除操作者的主观性。在此不再举例说明。
1.3.4质控图
通过以上三步骤,可以开始作室内质控图,根据RCVK的和SD作质控框图。利用质控
图可以对每次检验的结果进行监测,当没有更换另一批号试剂盒和另一批号质控血清时,
该质控图可以连续作下去。
质控血清的S/CO值低于-2SD的范围,属"告警",应寻找原因并在质控图上记录查出的
原因。
ELISA试验中,各种检验项目的误差允许范围均有待在实践中得出结论,以上只是举
例说明质控方法,不是定论。2SD是一般公认的允许误差限度。每批测定放一份质控血清
时,一次超过2SD应作为"告警",二次超出2SD为"失控"。当质控过程中,出现失控时,出
现失控时,应查找原因,通常是试剂盒或质控血清失效造成。更换试剂盒或更换质控血
清,找出原因纠正后重新检验。如果检验结果仍达不到要求或找不到原因时,应重复进
行OCV的检验。如果OCV检验的结果仍是好的,说明常规操作出现问题。
一般认为:①一次超出3SD;②连续二次超出2SD;③3-5次连续处于一侧的2SD之内;
④5~7次连续偏向横轴的一侧,均为失控。
第③、④种情况,单独依靠记录往往是不易察觉的,但在质控图上可以清晰地发现这种失
控。
1.3.5统计学计算方法--"即刻性"质控
以上介绍的质控方法基本上与临床化学测定的质控方法相同,但ELISA有其特殊性,
最合适的质控方法尚待研究建立。有些实验室不是每天进行ELISA项目的检验,而ELSIA
试剂盒效期短,用一批号试剂盒连续常规测20次,难度较大。采用"即刻法"质控统计方
法,只需连续测3次,即可对第3次检验结果进行质控。
"即刻法"的建立具体计算方法如下:
1)先将测定值从小到大排列
2)计算X和SD。
3)计算SDI上限和SDI下限值。
4)将SDI上限、SDI下限值与SDI值中的数字比较。当SDI上限值和SDI下限值<n2SD时,表
示处于控制范围内,可以继续往下测定,继续重复以上各项计算;当SDI上限和SDI下限
有一值处于n2SD和n2SD值之间时,说明该值在2SD~3SD范围,处于"告警"状态;当
SDI上限和SDI下限有一值>n2SD时,说明该值已在3SD范围之外,属"失控"。数值处
于"告警"和"失控"状态应舍去,重新测定该项质控血清和病人样本。舍去的只是失控
的这次数值,其他次测定值仍可继续使用。
即刻性质控统计方法,适于ELISA测定的质控。
当检测的数值超过20次以后,不必再使用"即刻法"质控统计计算,可以转入常规的质
控图的质控。将前20次的数值求出的和SD作质控框架图,第21次的数值,依次点入即
可。
1.4室间质量评价(external quality assessment,简称EQA)
室间质量评价简称室间质评,是由质控中心采用一系列的办法连续地、客观地评价各
实验室的试验结果,并发现室内质控不易发现的不准确性,了解各实验室之间结果的差
异,并帮助校正,使具有可比性。各实验室试验结果报到质控中心,经过统计分析,得出
相互比较的结果。这种评价不能控制各实验室每天发出的检验报告,而是一种回顾性评
价。室内质控主要监测试验结果的精密度,而室间质评主要控制试验结果的准确度,不能
互相替代。参与质评的实验室应先做好室内质控。
1.4.1室间质评的方法
1、发质控物进行调查
这是国内外室间质评的常用形式。部临检中心对乙肝标志物ELISA检验的室间质评采
用定期发放质控物至各实验室,各实验室在规定的日期进行检验,并将检验结果报至部临
检中心。部临检中心经统计分析,将评价结果寄回各实验室。通过评价,各实验室了解本
室工作质量,发现差距,并设法改进,以不断提高检验质量。
这种评价方式有一定缺点,即各实验室常对质控物特殊对待,在检验时选用特殊试剂
盒,选派特别的技术员进行检验,有的实验室互相和对结果并作修改。这就使EQA的结果
不能反映该实验室日常工作水平。
2、派观察员到实验室进行试剂调查
这种调查事先不通知,临时派观察员到实验室,指定采用常规方法,检验规定的一组
标本,进行评价。
ELISA实验步骤有哪些
ELISA实验原理是酶分子与抗体或抗抗体分子共价结合,此种结合不会改变抗体的免疫学特性,也不影响酶的生物学活性。
酶标记抗体可与吸附在固相载体上的抗原或抗体发生特异性结合。滴加底物溶液后,底物可在酶作用下使其所含的供氢体由无色的还原型变成有色氧化型,出现颜色反应。
因此,可通过底物的颜色反应来判定有无相应的免疫反应,颜色反应的深浅与标本中相应抗体或抗原的量呈正比。此种显色反应可通过ELISA检测仪进行定量测定,这样就将酶化学反应的敏感性和抗原抗体反应的特异性结合起来,使ELISA方法成为一种既特异又敏感的检测方法。
ELISA实验步骤及注意事项:
1、固相载体选择
聚苯乙烯:具有较强的吸附蛋白质的性能,抗体或抗原吸附其上后仍保留原来的免疫学活性。
聚氯乙烯:聚氯乙烯对蛋白质的吸附性能比聚苯乙烯高,但空白值也略高。
良好的ELISA板应该是吸附性能好,空白值低,孔底透明度高,各板之间、同一板各孔之间性能相近。
2、包被
①板孔的选择:ELISA级别的微孔板。
②抗体选择:选择支持ELISA实验的抗体,根据推荐浓度稀释或摸索最适浓度。
③包被缓冲液:pH9.6碳酸盐缓冲液或pH7.2磷酸盐缓冲液。
④包被温度:2-8℃过夜包被或室温(37℃)包被2h。
⑤包被浓度:包被浓度随载体和包被物的性质可有很大的变化。一般包被浓度为10ug/ml-20ug/ml。
3、封闭
①包被之后一定要立即封闭(封闭非特异性抗体)。
②选择效果较好的封闭剂(细胞培养级BSA、Tween等)。
4、加样及孵育
①加样时应将所加物加在ELISA板孔的底部,避免加在孔壁上部,并注意不可溅出,不可产生气泡。
②孵育的时间及温度参考试剂盒说明书。如有条件,建议加样孵育时使用shaker震荡仪,推荐轨道直径3mm,转速在500±50rpm。
③检测抗体、酶标物的稀释比例、孵育温度、孵育时间严格根据说明书提示。
④洗板对于ELISA来说,是极其关键的一步,保证ELISA的特异性。
⑤封板膜一定要一次一换,切勿二次甚至多次使用,以防交叉污染。
5、显色和终止
①使用前需检查,底物在加入96孔板之前应为无色透明。
②显色底物需现配现用,避免污染。
③孵育时间,说明书上为参考范围,具体需要根据实验条件自行摸索。可参考标曲浓度最大孔的颜色,变为蓝色较明显时即可。
ELISA实验检测抗体的实验步骤
操作步骤:
(1)将特异性抗原与固相载体联结,形成固相抗原。洗涤除去未结合的抗原及杂质。
(2)加稀释的受检血清,保温反应。血清中的特异抗体与固相抗原结合,形成固相抗原抗体复合物。经洗涤后,固相载体上只留下特异性抗体,血清中的其他成份在洗涤过程中被洗去。
(3)加酶标抗抗体,主要根据你的一抗来确定二抗用什么。可用酶标抗人Ig以检测总抗体,但一般多用酶标抗人IgG检测IgG抗体。固相免疫复合物中的抗体与酶标抗体抗体结合,从而间接地标记上酶。洗涤后,固相载体上的酶量与标本中受检抗体的量正相关。
(4)加底物显色
间接法由于采用的酶标二抗是针对一类免疫球蛋白分子(如抗人IgG),因此该法只需要换固相抗原,即可用一种酶标二抗检测各种与抗原相应的抗体,具有更广泛的通用性。
本法主要用于对病原体抗体的检测而进行传染病的诊断。间接法的优点是只要变换包被抗原就可利用同一酶标抗抗体建立检测相应抗体的方法。
如果有其他问题,可以联系我,呵呵!
elisa实验步骤和每步原理
ELISA酶联免疫吸附实验
1.原理:免疫分析是一种利用特定抗体与抗原或半抗原发生的高选择性高特异性识别和结合原理,对待测抗体或者抗原进行分析测定的方法,酶联免疫吸附分析(下称ELISA)是免疫分析的一种,分三个部分组成:免疫识别,信号输出和数据处理。
2.步骤:免疫识别是在聚苯乙烯制成的96孔板上包被抗体,而后利用抗体识别待测的抗原(通常是疾病的蛋白质生物标记物,病毒,细菌等等,从复杂待测液中将抗原吸附到96孔板表面。接着用带有辣根过氧化酶(Horseradish Peroxidase, HRP)、荧光或放射性标记的抗体通过直接或者间接的方式输出识别信号。最后利用信号强度,标准样品浓度梯度等信息计算得出待测样中目标抗原的浓度。
3.分类:根据免疫识别和信号输出方式的不同,ELISA可以分为双抗体夹心法、直接免疫竞争法和非直接免疫竞争法等等。其中双抗体夹心法在商业应用上最常见。
双抗体夹心法:
①:抗体包被在96孔板上包被抗体。由于酶标板是由聚苯乙烯制成,其含有的苯环与抗体的氨基酸残基具有类似π-π堆积作用的引力,结合静电和疏水作用,可以将抗体吸附于其表面。然后,将未吸附的抗体用缓冲液清洗后,加入含有明胶或牛血清蛋白(Bovine Serum Albumin, BSA)的封闭液以封闭酶标板上未结合抗体的部分。加入封闭液的目的,是防止其他蛋白因静电或疏水作用吸附在96孔板上,造成假阳性信号,干扰后续实验的进行。
②:免疫识别在96孔板上包被抗体后,加入待测样,并在37°C环境下孵育一段时间,通常是1-2小时。此时酶标板上的抗体与待测抗原进行特异性识别结合。此处抗体的质量是关键,好的抗体既能特异性高效地结合抗原又不受待测样中其他生物大分子、蛋白质和无机盐等成分的影响。
③:洗板将未结合的抗原洗掉,加入该抗原所对应的识别抗体并在37°C下继续培养1-2小时,接着将未连接上抗原的抗体洗掉。
④:酶标信号输出加入带有辣根过氧化酶(Horseradish Peroxidase, HRP)标记的酶标二抗,用于和标准抗体结合。在培养30分钟后洗掉未连接的二抗,并加入显色剂显色。根据显色的结果判断抗原的浓度。一般认为,抗原浓度与显色后的发光强度呈正相关。
免疫竞争法
以抗原竞争抗体为例,在上述免疫夹心法操作步骤的第二步加入待测抗原后,立刻加入酶标抗原,使之与待测抗原竞争识别酶标板上的抗体。当待测抗原浓度越高,能够连上酶标板上抗体的酶标抗体就越少,输出的信号就越少。这样待测样浓度与酶显色信号就呈逆相关。
如果你还想了解更多这方面的信息,记得收藏关注本站。
与本文知识相关的文章:



